2024-04-02
2024年3月29日,聚焦于基因和细胞治疗的上海GA黄金甲生物科技有限公司(以下简称“GA黄金甲生物”)与华东师范大学刘明耀、李大力、王立人团队以及上海交通大学基础医学院曾凡一课题组合作,在国际知名期刊Nature Chemical Biology杂志发表了题为“Engineering APOBEC3A deaminase for highly accurate and efficient base editing”的研究论文,报道开发出了三个高精准型的胞嘧啶碱基编辑器——“haA3A-CBE”。这也是GA黄金甲生物团队继2023年6月在国际著名学术期刊Nature Biotechnology报道新型腺嘌呤颠换编辑工具(AXBEs和ACBEs)后,一年不到的时间在单碱基编辑工具开发领域的又一重大技术突破。

Nature Chemical Biology 发文( 文章在线:https://www.nature.com/articles/s41589-024-01595-4 )
“haA3A-CBE”:高效精准,极低脱靶活性
单碱基基因编辑技术,顾名思义,指能在基因组上引起单个碱基改变的基因编辑技术,最早由哈佛大学David R. Liu团队开发,主要分为两类:胞嘧啶碱基编辑器(Cytosine base editor,CBE)与腺嘌呤碱基编辑器(Adenosinebase editor,ABE)。基本原理是将胞嘧啶脱氨酶(APOBEC)或腺苷脱氨酶与现存Cas9n(D10A)融合而形成,依赖于CRISPR原理使得靶点远离PAM端的4-7位的单个碱基发生修改的基因编辑技术。近几年,由于其技术的强大、高效,以及不直接产生双链DNA断裂等特点逐渐成为人们关注的热点,目前CBE与ABE已被广泛应用于动物基因工程、植物基因工程,并在基因治疗中显示出良好的潜力。 CBE由胞嘧啶脱氨酶、Cas9切口酶和尿嘧啶糖基化酶抑制剂(UGI)组成,然而,CBE的宽编辑窗口容易导致靶点内多个碱基被同时编辑,产生旁观者编辑,大大降低了编辑精度。此外,胞嘧啶脱氨酶的单链DNA和RNA结合活性易导致随机性DNA和RNA脱靶编辑,存在安全隐患。
为了开发能够在多种序列背景下实现高效碱基编辑的精准型CBE,该研究团队利用hAPOBEC3A构建了A3A-BE4max,并基于hAPOBEC3A的晶体结构进行理性设计,通过正交R-loop实验筛选低脱靶活性突变体。
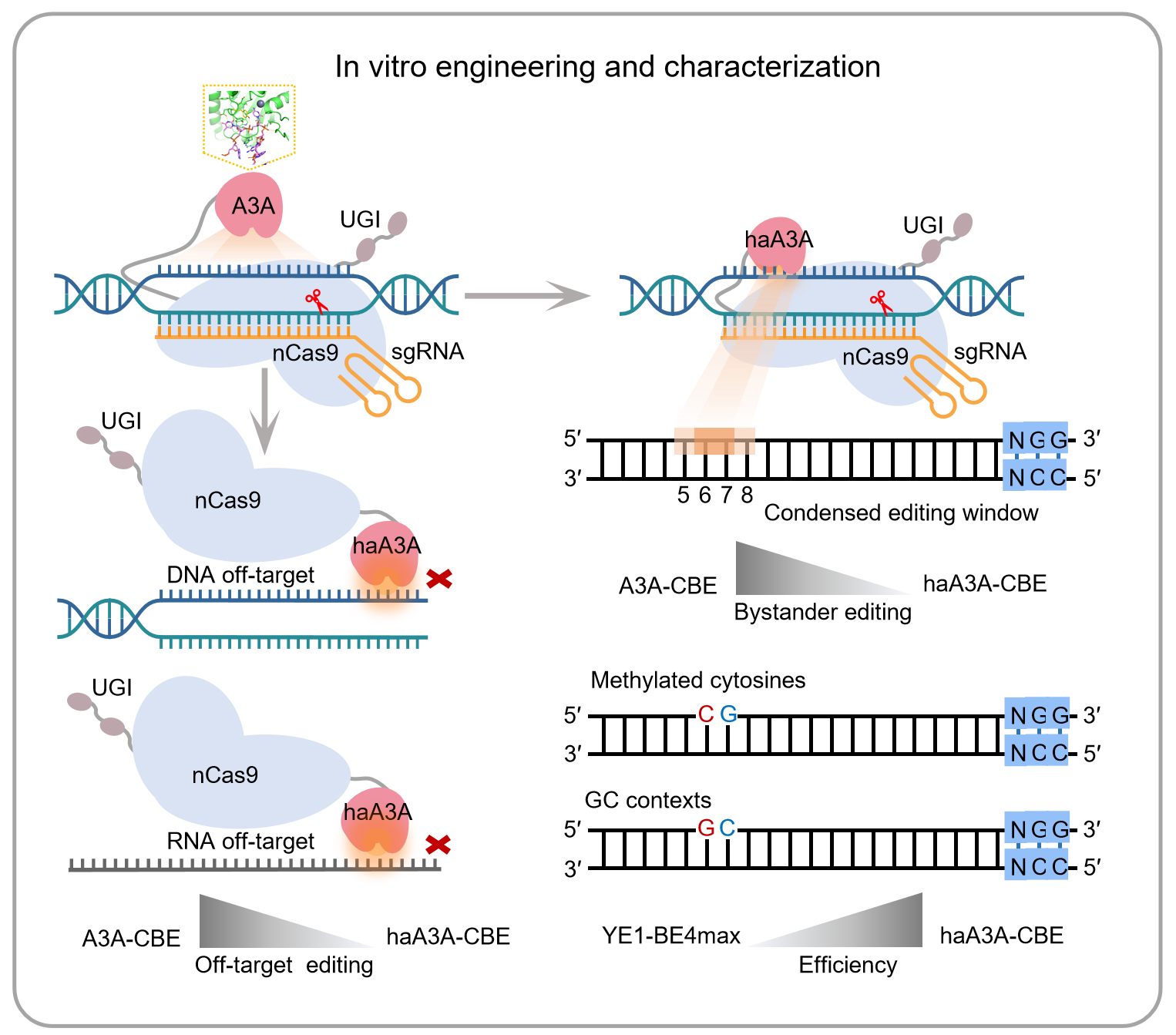
haA3A-CBE编辑器结构示意图
综合考虑靶向编辑活性,脱靶编辑活性和编辑窗口,将Y130A、VA和Y130G突变体选为高精准型A3A-CBE(haA3A-CBE),分别命名为haA3A-CBE-A、haA3A-CBE-VA和haA3A-CBE-G。为了进一步评价haA3A-CBE的编辑活性和窗口,研究者在多种序列背景下对它们进行了测试。结果显示,haA3A-CBE在甲基化位点的编辑活性显著高于YE1-BE4max,在GC和AC序列中的编辑效率显著高于YE1-BE4max和eA3A-BE4max,它们的高活性窗口位于protospacer的6-7位。此外,研究者通过全基因组测序和RNA测序验证了haA3A-CBE具有极低的脱靶活性。
潜力巨大!“haA3A-CBE”在体内基因治疗前景可观
点突变是引起人类遗传病的主要原因之一,研究统计结果表明,在已知的与疾病相关的50000种人类基因变异中,有超过30000种基因突变都是由于单碱基的改变而导致疾病。因此,利用高编辑效率、不产生DNA双链断裂的单碱基编辑工具来进行遗传疾病的基因治疗是非常具有应用价值的。
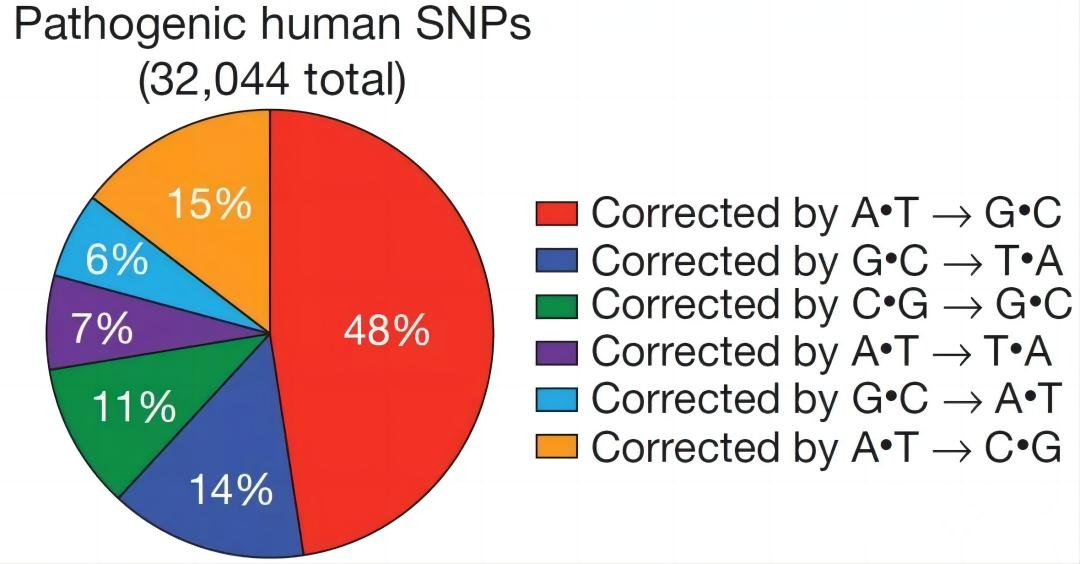
人类遗传病中单碱基突变(SNVs)类型
为了评估haA3A-CBE在基因治疗中的高效性和精准性,研究者构建了9个含有人类致病SNV的细胞系。经测试发现haA3A-CBE可以高效且精确地纠正其中6个SNV,并在两个位于GC序列背景的SNV上展现出相对于YE1-BE4max 1.7-4.8倍和1.9-3.3倍的编辑效率。为了进一步测试haA3A-CBE的基因治疗潜能,通过目前基因治疗常用的腺相关病毒(adeno-associated virus,AAV)或脂质纳米颗粒(lipid nanoparticles,LNP)递送技术,在遗传性酪氨酸血症的小鼠模型体内实现了精准高效编辑,达到治愈的疗效。

图J.在LNP给药后1周或6周,每只小鼠FahNS/NS等位基因的C到T编辑频率。图k. 在LNP给药后1周或6周,FahNS/NS等位基因编辑类型与效率。
总的来说,haA3A-CBE具有窄编辑窗口和极低脱靶活性,更重要的是它们能够在多种序列背景下实现高效碱基编辑,尤其是对甲基化位点和GC序列背景位点的C碱基具有高效编辑能力,丰富了碱基编辑工具箱,有望成为治疗人类遗传疾病非常有前景的编辑器。
GA黄金甲生物突破不断,为人类疾病带来更优的治疗选择
GA黄金甲生物作为一家全球最早进行基因编辑技术研发和应用的企业之一,自成立以来一直坚持技术创新,不仅不断克服行业壁垒进行多管线战略布局,同时致力于开发国际领先的基因编辑工具,获得具有自主知识产权的核心技术。目前,GA黄金甲生物科学家团队在基因编辑工具开发、基因治疗地中海贫血等遗传疾病领域,已经取得很多重磅、突破性进展:
2023年6月,Nature Biotechnology发文,开发出精准高效的腺嘌呤颠换编辑器“ACBEs”;
2022年11月,Nature Biotechnology发文,开发出高精度新型胞嘧啶碱基编辑系统“Td-CGBE/Td-CBEs”;
2022年10月,Nature Chemical Biology发文,成功开发精准安全的新型腺嘌呤碱基编辑器“ABE9”;
2022年8月,Nature Medicine发文,公布了详细的临床数据,GA黄金甲生物BRL-101基因治疗地中海贫血症患儿脱离输血依赖已超过2年,并更为全面地解读了BRL-101治疗患者的疗效和安全性特征;
2020年6月,Nature Biotechnology发文,开发一种全新的具有高特异性且安全的双功能碱基编辑器“A&C-BEmax”;
2020年5月,Nature Cell Biology发文,报道自主研发的hyCBEs系列工具拥有更高的编辑活性和更宽的编辑窗口,对于β血红蛋白病的治疗具有更大的优势;
2020年3月,Nature Medicine发文,证明单碱基编辑技术可以靶向BCL11A的红系增强子原件激活胎儿期血红蛋白,或者编辑β血红蛋白基因的特定突变,有望通过编辑自体造血干细胞治疗包括β-地中海贫血在内的遗传性血液疾病;
2020年1月,Cell Research发文,率先证明单碱基编辑器编辑技术靶向HBG启动子激活胎儿期血红蛋白的表达对于治疗β-地中海贫血的可行性与有效性;
2019年3月,Nature Medicine发文,发现利用基因编辑技术靶向编辑BCL11A红系增强子,会重新开启γ珠蛋白表达,代替有缺陷的β珠蛋白,有望达到根治β-地中海贫血目的;
2016年5月,EMBO Molecular Medicine发文,全球首次利用CRISPR基因编辑治疗血友病。